الغاز الرجعي المكثف
خصائص النفط - الغاز الرجعي المكثف
توجد بعض مخاليط الهيدروكربونات بشكل طبيعي فوق درجة حرارتها الحرجة مثل مكثفات الغاز. عندما ينخفض الضغط على هذه الخلائط، فبدلاً من التمدد (إذا كانت غازية) أو التبخر (إذا كانت سائلة) كما هو متوقع، فإنها تميل إلى التكاثف. وعلى العكس من ذلك، عند زيادة الضغط، فإنها تتبخر بدلاً من أن تتكثف. يتم توضيح العملية من خلال حالة درجة الحرارة Tr3 في الشكل اللاحق، ومنحنى تكاثف الغاز في الشكل التالي. تحدث هذه العملية بسبب قوى تؤثر على جزيئات ذات أحجام مختلفة وتعتمد على توازن هذه القوى، كما هو موضح في الشكل.
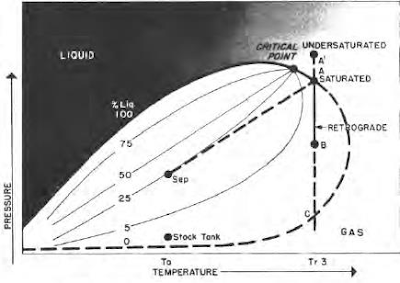 |
| رسم تخطيطي لطور الغاز الرجعي المكثف |
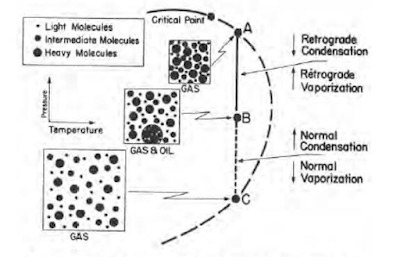 |
| السلوك الرجعي المتوازن للغاز المتكثف |
من ناحية أخرى، يعتمد التبخر والتكثيف الطبيعي بشكل أكبر على التوازن بين القوى الجزيئية للجزيئات المكونة ذات الحجم المماثل.
عندما ينخفض الضغط (عند درجة حرارة ثابتة) إلى ما دون ضغط نقطة الندى (A)، فإن الجذب بين جزيئات المكونات الخفيفة والثقيلة يتناقص لأن الجزيئات الخفيفة تتحرك بعيدًا عن بعضها البعض.
وعندما يحدث هذا، يصبح التجاذب بين جزيئات المكونات الثقيلة أكثر فعالية؛ وبالتالي، تتجمع هذه الجزيئات الثقيلة لتشكل سائلًا. وتستمر هذه العملية حتى يتم الوصول إلى الضغط (B) حيث يتكون الحد الأقصى لكمية السائل. يسمح المزيد من الانخفاض في الضغط للجزيئات الثقيلة ببدء التبخير الطبيعي، وهي العملية التي يتم من خلالها اصطدام عدد أقل من جزيئات الغاز بسطح السائل؛ يؤدي هذا إلى مغادرة المزيد من الجزيئات بدلاً من دخولها إلى الطور السائل، حتى يحدث التبخر الكامل للسائل مرة أخرى (C).
الغاز الرطب
يظهر سلوك الغاز الرطب في الشكل التالي، حيث تكون درجة الحرارة أعلى من درجة حرارة التكثيف الحرجة لخليط الغاز. ولذلك، فإن انخفاض الضغط (من A إلى B) لن يسبب تكثيف السائل. ومع ذلك، فإن مرور الغاز من درجة الحرارة الحالية إلى ظروف خزان المخزون حيث تكون درجة الحرارة أقل، سيؤدي إلى تكوين السائل. يحدث هذا بسبب انخفاض كافٍ في الطاقة الحركية للجزيئات الثقيلة مع انخفاض درجة الحرارة وتحولها اللاحق إلى سائل من خلال قوى التجاذب بين الجزيئات.
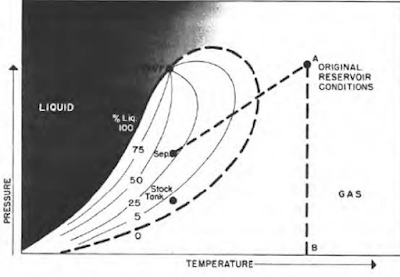 |
| رسم تخطيطي لمرحلة الغاز الرطب |
الغاز الجاف
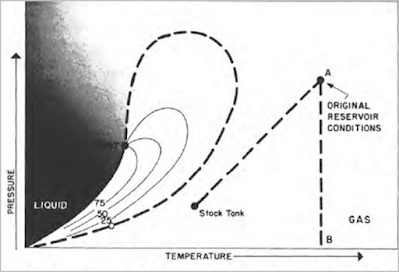 |
| رسم تخطيطي لمرحلة الغاز الجاف |
كلمات مفتاحية/ الغاز رطب، الغاز جاف، الغاز المكثف، مكثفات النفط، المكثفات.


تعليقات